Innovative Reagenzien und neue Gerätetechnologie von Cytecs ermöglichen erhebliche Kostensenkungen sowie den flächendeckenden Einsatz auch in infrastrukturschwachen Regionen / Zulassung als IVD-Produkt bereits erfolgt
Münster – July 29, 2020: Das deutsche Diagnostikunternehmen Cytecs vermeldet die Einführung eines neuen Tests zum molekulardiagnostischen Nachweis des Covid-19-Infektionserkrankungen auslösenden Coronavirus SARS-CoV-2.
Der neue Test wurde bereits erfolgreich über die Bezirksregierung Münster gemäß der EU-Verordnung zu In-vitro-Diagnostika (IVD) angemeldet und ist damit seit dem 20. Juli 2020 als IVD-Produkt in Deutschland und darüber hinaus in den meisten Ländern weltweit offiziell zugelassen. Die im Rahmen dieser Anmeldung vorzulegenden Vergleichsuntersuchungen belegen die Gleichwertigkeit der Qualität und Zuverlässigkeit der Ergebnisse des von Cytecs nunmehr neu eingeführten Tests im Vergleich zu den konventionellen sog. „Real-Time RT-PCR“-Verfahren.
Mit dem neuen Verfahren wird eine deutliche Reduktion der gesamten Reagenzienkosten pro Test auf nicht mehr als 8 Euro erreicht, während sich die Kosten für die dazugehörige Geräteausstattung der von Cytecs ebenfalls neu entwickelten, innovativen und portablen molekulardiagnostischen Gerätetechnologie auf lediglich 10.000 Euro belaufen. Der Probendurchsatz liegt bei bis zu 600 Tests am Tag. Auf Basis der sehr niedrigen Gerätekosten ist eine Multiplikation des Probendurchsatzes sehr einfach realisierbar.
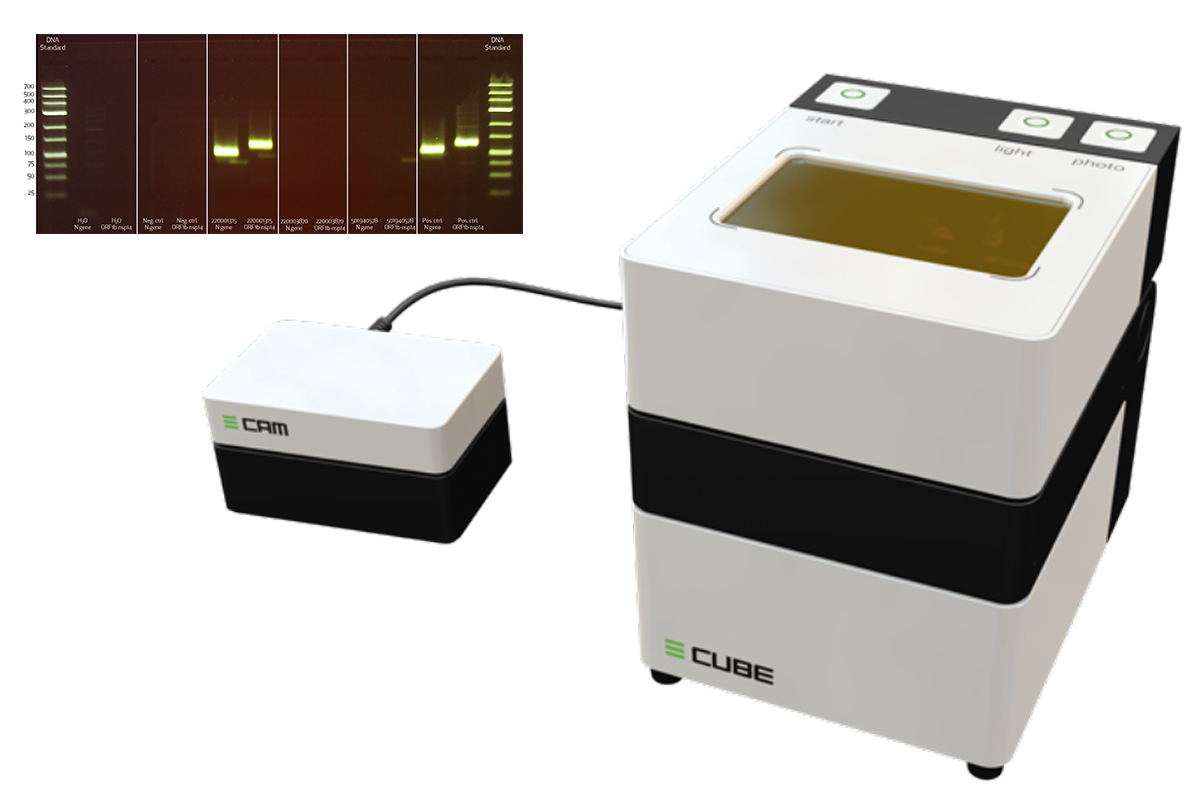
Das Verfahren basiert auf der Amplifikation von zwei SARS-CoV-2 Gensequenzen nach Umschreibung der Virus-RNA in die komplementäre DNA. Diese wird anschließend mit einem DNA-spezifischen Fluoreszenzfarbstoff markiert und mit Hilfe des von Cytecs neu entwickelten ultrakompakten sowie auch dezentral einsetzbaren „all-in-one“ Gelelektrophorese-Systems E-CUBE analysiert. Während für den Cytecs-Test die gleichen molekularbiologischen Ansätze wie bei konventionellen Tests der Real-Time RT-PCR-Methode verwendet werden, ist dagegen der zytochemische Nachweis der Nukleinsäureamplifikate neuartig.
Zudem sind die ansonsten überaus temperatursensiblen Reagenzien für den SARS-CoV-2-Nachweis nunmehr erstmals als lyophilisierte, also gefriergetrocknete Substanzen verfügbar. Kühlketten und Kühllagerung sind auf Basis des neuen Cytecs-Tests somit nicht mehr erforderlich, was die bislang üblichen, sehr großen Herausforderungen und Probleme bei Versendung und Einsatz von konventionellen molekulardiagnostischen Reagenzienkits in entlegenen wie auch warmen Regionen der Erde eliminiert.
Vorteilhaft an dem neuen Verfahren ist weiterhin, dass die notwendigen konventionellen PCR-Geräte („Thermocycler“) und Gelelektrophorese-Geräte bereits zur Standardausstattung der meisten Labore in Forschungseinrichtungen und größeren Krankenhäusern gehören – in Industrieländern wie auch beispielsweise in Subsahara-Afrika. Eine Neuanschaffung von Analysegeräten für den neuen SARS-CoV-2-Test von Cytecs erübrigt sich daher in vielen Fällen, genauso wie – bei Einsatz sowohl von vorhandenen Geräten wie auch der Cytecs-Gerätetechnologie – das Erfordernis einer Neuinstallation durch extra zu entsendende Techniker.
In diesen Tagen berichtet die Weltgesundheitsorganisation WHO über eine viertel Million Corona-Neuinfektionen weltweit pro Tag. Die überaus dynamische Ausweitung der Pandemie betrifft in besonderem Maß ärmere Länder, in denen die Gesundheitssysteme auf eine solche Entwicklung kaum vorbereitet waren und bezüglich der dringend benötigten Laborinfrastruktur und -ausstattung ohne innovative Ansätze zeitnah wohl auch nicht hinreichend bedarfsgerecht nachgerüstet werden können.
Im Vordergrund der Entwicklung des neuen Tests von Cytecs stand insofern, die Problematik zu adressieren, dass den meisten Entwicklungs- und Schwellenländern bisher keine ausreichenden Testkapazitäten zur Bekämpfung und Kontrolle der Coronavirus-Pandemie zur Verfügung stehen. In diesem Kontext verfügt Professor Dr. Wolfgang Göhde, Geschäftsführender Gesellschafter der Cytecs GmbH, über eine 20-jährige Erfahrung bei der Entwicklung von neuen Diagnosekonzepten für große Infektionskrankheiten, insbesondere auch in infrastrukturschwächeren und ärmeren Ländern. Gemeinsam mit der Biologin Dr. Dr. Hildegard Göhde hatte Wolfgang Göhde 1967 die Firma Partec GmbH in Münster gegründet, im Jahr 2000 dann gemeinsam mit seinem Sohn Roland Göhde das Diagnostikunternehmen, das 2011 zur Partec GmbH in Görlitz wurde. Ab dem Jahr 2000 gelang es Partec, die für eine erfolgreiche Behandlung von HIV/AIDS-Infizierten unverzichtbar lebenslang erforderliche Immunstatusdiagnostik über neue, innovative und erstmals mobil einsetzbare Gerätetechnologien und neuartige Reagenzien – im Vergleich zu den seinerzeit üblichen Tests um einen Faktor 20 reduziert – so preiswert anzubieten, dass diese Diagnostik für alle Betroffenen erreichbar und auch bezahlbar wurde. Infolgedessen konnte Partec weit über 100 Länder, insbesondere in Afrika und Asien, mit der entsprechenden Labortechnik ausstatten und bis zu 5 Millionen kostengünstige Tests im Jahr liefern. Die langjährig gesammelten, intensiven vor-Ort-Erfahrungen waren Grundlage und Motivation dafür, nunmehr eine innovative Diagnostiklösung zu entwickeln und zu etablieren, die eine hochsensitive, verlässliche Detektion des Coronavirus SARS-CoV-2 auch unter erschwerten Laborbedingungen ermöglicht.
Kontakt:
Cytecs GmbH
Im Derdel 8
DE-48161 Münster | Deutschland
Tel: +49 (0) 2534 97736-0
Fax: +49 (0) 2534 97736-29
info@cytecs.com